[جمع بندی]
کتابی که بخواهد، توسط علم الهی، تمام تکوین بلکه نفس الامر را تدوین کند، چارهای نیست که از نشانههای چندین منظوره استفاده کند، و لذا قرآن کریم به لسان عربی که رسمِ واوِلعلامتی دارد (نه واوِلحرفی[1]) نازل شده است،
[تکوین چند منظوره]
[پیوند کووالانسی]
اگر در تکوین نمونههایی داریم مثل پیوند شیمیایی کووالانسی که یک الکترون نقش چندگانه دارد[2] آیا موافقت تدوین با تکوین چگونه باید صورت گیرد؟
[تدوین چند منظوره]
[مثال: مکعب روبیک]
مثلا بالعیان میتوان دید که در مکعب روبیک[3]، یک مهره مشتمل بر چند رنگ است، و هر رنگ نقش ایفا میکند، و هر رنگ که در بالا قرار گرفت و روز ظهور او شد در همین حال رنگهای دیگر را در باطن خود دارد! این یک مثال جسمانی و فیزیکی است که اگر راهبر به عالم معانی باشد افق عجائب ترفندهای نگاشتِ تکوین و نفس الامر را در الواح الهیه نمایان میسازد.
بنده چنین فکر میکنم که رمز اتفاق جمیع مسلمین در طول تاریخ بر ترویج تعدد قرائات! -یعنی نه تنها بر عدم منع بلکه بر ترویج آن! -امری صحیح و مطابق شأن عظیم کتاب مبین است، فقهای شیعه نقل اجماع کردند بر جواز قرائت در نماز به قرائت یکی از قراء سبعه[4]، و ظاهر آن این است که یعنی حتی در یک نماز! در یک رکعت یک قرائت و در رکعت دیگر قرائت دیگر! و این منافات ندارد با حدیث: «انما هو واحد نزل من عند واحد[5]»، چون باید منظور از این حدیث را در کنار سبعه أحرف فهمید، اگر به صدها تفسیر شیعه و سنی مراجعه کنید میبینید مرتب مسأله تعدد قرائات را ذکر میکنند و مخاطبین خود را مأنوس این فضا میگردانند، و محال است امری مورد رضایت قطعی مولا نباشد و تمام مسلمین بر خلاف آن اجماع کنند.
[اشکال]
درباره امتیاز چندمنظوره بودن زبان عربی به نقش اعراب و نقطه اشاره کرده اید. سوال بنده این است که این ظاهرا در حد یک موید بحث شما بود نه رکن اصلی استدلال؟ درست است؟ زیرا هم در نقلهای از مصاحف ابن مسعود و از ائمه کلمات اضافه هم وجود دارد و هم در همین قرائات سبعه موجود در نزد ما کلمات کم و زیاد وجود دارد. مثلا در قرائت ورش از نافع که ظاهرا دومین قرائت به لحاظ شهرت است در آیه23 سوره حدید (فَإِنَّ اللَّهَ هُوَ الْغَنِيُّ الْحَمِيدُ ) کلمه «هو» را ندارد[6] .
[پاسخ]
درست است که کوچ کردن حروف مصوّت از پایه کلمه به موضع حرکات، فقط در محدوده ثبات پایه و حروف صامت آن معنا مییابد و نمیتواند مصحح قرائاتی که در پایه مشترک نیستند بشود، اما نکته مهم این است که اگر ثبوتا فهمیدیم که میتواند این انعطاف در وجوه مختلف یک پایه، همگی از ناحیه ملک وحی، سر و سامان یابد، و رأس مخروط یک آیه به عنوان یک نقطه بسیط، به صورت تدوین تکوین، منبسط شود، و در انبساط خود، همه وجوه، دفعتا توسط ملک وحی، قرائت شود، و تمانعی در کار نباشد، زمینه درک تعدد قرائت ملک وحی، نسبت به پایههای همموضع، فراهم میشود.
و دراین تاپیک هم بحث مناسب اینجا صورت گرفته است[7].
[1] یعنی مصوّت ها در آن نه به صورت یک حرف بلکه به صورت علامت بر روی پایه حروف همخوان استفاده می شوند و توضیح این مطلب گذشت.
[2] پیوند کووالانسی (به انگلیسی: Covalent bond) یا رابطه اشتراکی یا بند همارزا یک نوع رابطه شیمیایی در شیمی است. در ترکیب یونی، اتمها با از دست دادن یا گرفتن الکترون، مدار بیرونی خود را پر میکنند. اما در رابطه اشتراکی (کووالانسی) اتمها میتوانند با اشتراک الکترونها مدار خودشان را پر کنند و به آرایش هشتایی پایدار گاز نجیب بعد از خودشان برسند پیوند کووالانسی بین نافلزات مشابه یا غیرمشابه با اشتراک الکترونهای مدار آخر انجام میشود. پیوند کووالانسی را با خط راست نشان میدهند و در هر پیوند(۲)الکترون شرکت دارند. پیوند کووالانسی میتواند《یکگانه، دوگانه یا سهگانه》باشد. موادی که پیوند کووالانسی دارند در هیچ شرایطی برق را عبور نمیدهند؛ البته گرافیت از این قضیه مستثنی است. موادی که پیوند کووالانسی دارند نقطه جوش و ذوب پایینتری نسبت به موادی با پیوند یونی دارند و بین آنها هر کدام که جرم مولکولی بیشتری دارد دارای نقطه جوش و ذوب بالاتری است. به جز هیدروژن در بقیه اتمها مجموع الکترونهای پیوند و غیر پیوندی در لایه ظرفیت باید هشتایی باشد. تمام گازها، قندها، الکلها، پلیمرها، سوختها و آب پیوند کووالانسی دارند. پیوند کووالانسی نیروی جاذبه بسیار قوی دارد که اتمها را به شدت کنار هم نگه میدارد، به همین خاطر به ترکیب مولکولی معروفند. البته شایان ذکر است که آب فراوانترین ترکیب مولکولی است که به سه حالت جامد مایع وگاز یافت میشود. نام دیگر این پیوند اشتراکی نیز است.
کلیات
پیوند کووالانسی در اثر نیروی جاذبهٔ الکتریکی به وجود میآید؛ به طور مثال هنگامی که دو اتم هیدروژن به هم نزدیک میشوند، جاذبهٔ الکتریکی بین آنها ایجاد میشود و دو اتم با همرسانی یک جفت الکترون کنار هم میمانند. پیوند کووالانسی اغلب بین دو اتم نافلز است؛ مثلاً یک اتم کربن با چهار اتم هیدروژن چهار پیوند کووالانسی در یک مولکول به وجود میآورند که به متان معروف است.
پیوند کووالانسی پیش از ۱۹۲۶
بر اساس نظریه لوویس، پیوند کووالانسی نتیجه اشتراک یک جفت الکترون (=دو الکترون) بین دو اتم است. بر این اساس، الکترونهای مشترک توسط هسته هر دو اتم جذب میشوند و مانند چسب، منجر میشوند که دو هسته نزدیک به هم بمانند و اتمها به هم پیوند (اتصال) یابند. طبق نظریه لوویس، اتم هر عنصر تا جایی پیوند برقرار میکند که جمع الکترونهای پیوندی (=الکترونهای مشترک) و الکترونهای نا پیوندی آخرین لایه الکترونیاش برابر با ۸ شود (مشابه گازهای نجیب؛ به جز هیدروژن که همانند هلیم، و فقط دارای ۲ الکترون میشود). این قاعده به قاعده هشتتایی (هشتایی) یا همان اوکتت (Octet) معروف است. (سایت ویکی پدیا)
قاعده اکتت
قاعده هشتتایی (اکتت) بیان میکند برای اینکه مولکولها به پایداری برسند، باید در لایه ظرفیت تمامی اتمهای آنها، تعداد ۸ الکترون وجود داشته باشد که این ۸ الکترون میتوانند از طریق اشتراکگذاری، گرفتن یا از دست دادن الکترون بدست بیایند. در پیوند کووالانسی، اتمها تمایل دارند تا برای رسیدن به قاعده اکتت یا همان آرایش گاز نجیب، الکترونهای خود را به اشتراک بگذارند.
مقدمهای بر پیوند کووالانسی یا پیوند اشتراکی
اتم کلر با توجه به الکترونخواهی خود، به گرفتن یک الکترون و تکمیل آرایش الکترونی خود تمایل دارد. به نظر شما، این الکترون را از کدامیک از دو اتم سدیم یا هیدروژن، سادهتر میتوان بدست آورد؟ از هیچکدام از دو اتم نمیتوان به سادگی الکترون کسب کرد اما انرژی مورد نیاز برای جذب الکترون از سدیم (انرژی یونش) بسیار کمتر از انرژی مورد نیاز برای جذب هیدروژن است.
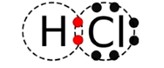
در حقیقت، هرقدر انرژی یونش کمتر باشد، خاصیت فلزی عنصر بیشتر میشود. در نتیجه، سدیم، خاصیت فلزی بیشتری از هیدروژن دارد. در حقیقت، هیدروژن را به عنوان عنصری نافلز در نظر میگیرند. اتم هیدروژن در حالت گازی، الکترونی را در اختیار اتم نافلز دیگری قرار نمیدهد. انجام پیوند بین یک اتم هیدروژن و یک اتم کلر، با اشتراک گذاشتن الکترون امکانپذیر است که به پیوند حاصل، «پیوند کووالانسی» (Covalent Bonding) میگویند. برای روشنتر شدن اشتراکگذاری الکترونها، بهتر است در خصوص ساختار لوییس مولکول HCl به بحث بپردازیم.
در تصویر بالا، خارجیترین لایه اتم توسط خطچینهایی نشان داده شده است. همچنین، الکترونهای لایه ظرفیت نیز توسط نقطههایی نمایش داده شدهاند. با دقت در این ساختار، درمییابیم که اتم هیدروژن، دو الکترون در لایه آخر خود دارد و آرایش لایه آخر آن مشابه با اتم هلیوم است. به همین صورت، اتم کلر، ۸ الکترون در لایه ظرفیت خود و آرایشی مشابه با آرگون دارد.
توجه کنید که در این شمارش الکترونها، الکترونهایی که با رنگ قرمز مشخص شدهاند را دو بار حساب کردیم، یک بار برای اتم هیدروژن و یک بار برای اتم کلر. این دو الکترون، بین دو اتم کلر و هیدروژن به اشتراک گذاشته شدهاند. به عبارت دیگر، این جفتالکترون اشتراکی، پیوند کووالانسی را تشکیل میدهد. در تصویر زیر، ساختارهای لوییس برای دو مولکول دیگر نمایش داده شده است:
همانند اتم کلر در HCl ، اتم اکسیژن در ساختارهای لوییس H2O و Cl2O، با هشت الکترون، احاطه شده است. توجه داشته باشید که اتم هیدروژن، نوعی استثنا است چراکه این اتم تنها ۲ الکترون را در لایه ظرفیت خود جای میدهد. ساختار لوییس به در فهم این موضوع کمک میکند که چرا عناصر هیدروژن و کلر به صورت مولکولهای دواتمی H2 و Cl2 وجود دارند. در هر دو مولکول، یک جفت الکترون بین دو اتم به اشتراک گذاشته شده است.(سایت فرادرس، مقاله پیوند کووالانسی به زبان ساده)
[3] مکعب روبیک یک جورچین (پازل) مکانیکی است که در سال ۱۹۷۴ توسط یک مجسمهساز و پروفسور معمار مجارستانی به نام ارنو روبیک ابداع شد. نام اصلی آن "مکعب جادویی" است که توسط مخترع آن نامگذاری شدهاست.
این اسباب بازی در سال ۱۹۸۰ به افتخار سازنده آن به "مکعب روبیک" تغییر نام یافت و برنده جایزه ویژه بهترین پازل جهان در آلمان شد و گفته شده پرفروشترین اسباب بازی جهان با ۳۵۰٫۰۰۰٫۰۰۰ عدد است.
در هر مکعب روبیک کلاسیک ۶ وجه و در هر وجه ۹ تکه و هر وجه دارای یک رنگ است، در نتیجه کلاً دارای ۶ رنگ (رنگبندی استاندارد: سفید، زرد، نارنجی، قرمز، آبی، و سبز) است. گفته میشود این مکعب دارای ۴۳ تریلیون جایگشت (تعداد ترکیبهای ممکن برای موقعیت رنگها) است؛ و معمولاً افراد به دو روش مبتدی و حرفهای آن را حل میکنند که روش مبتدی دارای ۷ مرحله است و این روش تقریباً دارای ۷ فرمول است اما روش حرفهای دارای ۴ مرحله و بیش از ۱۲۰ فرمول است
مکانیزم محوری این پازل به شما این امکان را میدهد که در هر وجه بهطور جداگانه رنگهای دیگر را به هم ریخت، و هدف از بازی این است که تمام رنگهای آن در وجه خود و به صورت درست در کنار هم قرار گیرند.
در سالهای بعد این مکعب گسترش یافت و مدلهای دیگری از آن درست شدهاست، از جمله: ۲×۲×۲ (مکعب جیبی، مینی مکعب یا مکعب یخی)، ۳×۳×۳ (مکعب استاندارد)، ۴×۴×۴ (انتقام روبیک، یا مکعب استاد) و ۵×۵×۵ (روبیک پروفسورها) و به تازگی اندازههای بزرگتر نیز درست شدهاند (۶x۶×۶ و ۷x۷×۷) و اندازه بزرگترین مکعب ثبت شده در گینس ۳۳x۳۳x۳۳ میباشد. رکورد سریعترین زمان حل مکعب روبیک متعلق به Yusheng Du با زمان ۳٫۴۷ ثانیه است.
[4] السّادس: يجوز أن يقرأ بأيّ قراءة شاء من السّبعة لتواترها أجمع، و لا يجوز أن يقرأ بالشّاذّ و إن اتّصلت رواية، لعدم تواترها و أحبّ القراءات إليّ ما قرأه عاصم من طريق أبي بكر بن عيّاش، و قراءة أبي عمرو بن العلاء، فإنّهما أولى من قراءة حمزة و الكسائيّ؛ لما فيهما من الإدغام و الإمالة و زيادة المدّ، و ذلك كلّه تكلّف، و لو قرأ به صحّت صلاته بلا خلاف.(منتهی المطلب، ج ۵، ص ۶۴-۶۵)
(ذخیرة المعاد فی شرح الارشاد، ج ٢، ص ٢٧٣)
و الحاصل أنّه لا إشكال في جواز موافقة قراءة السبع المشهورة كما دلّت عليه الأخبار المستفيضة إلى زمان ظهور القائم عليه السلام(غنائم الایام، ج ٢،ص ۵٠٢)
[5] ۱۲- الحسين بن محمد عن علي بن محمد عن الوشاء عن جميل بن دراج عن محمد بن مسلم عن زرارة عن أبي جعفر ع قال: إن القرآن واحد نزل من عند واحد و لكن الاختلاف يجيء من قبل الرواة.
۱۳- علي بن إبراهيم عن أبيه عن ابن أبي عمير عن عمر بن أذينة عن الفضيل بن يسار قال: قلت لأبي عبد الله ع إن الناس يقولون إن القرآن نزل على سبعة أحرف فقال كذبوا أعداء الله و لكنه نزل على حرف واحد من عند الواح(الكافي (ط - الإسلامية) ؛ ج2 ؛ ص630)
و قال الصادق- عليه السلام: «القرآن واحد، نزل من عند واحد على واحد، و إنما الاختلاف من جهة الرواة»( إعتقادات الإمامية (للصدوق) ؛ ص86)
[6] اشکال آقای سوزنچی با نام کاربری Hosein-
[7] برای مشاهده خلاصه مطالب مورد بحث و بررسی در تاپیک مورد نظر به پیوست این متن مراجعه فرمایید.

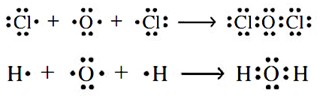
بدون نظر